Perfumes têm em sua composição álcool etílico
Álcoois são compostos orgânicos que contêm um ou mais grupos oxidrila (OH) ligados diretamente a átomos de carbono saturados.
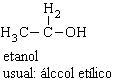
Observação:
Nem todos os compostos que apresentam o grupo oxidrila(OH), podem ser considerados álcoois.
CH2 = CH * Não é um álcool; é um enol (instável), pois o OH está ligado a um carbono insaturado.
|
OH
Cotidiano
No dia-a-dia quando os jornais, a televisão etc. falam em álcool, estão se referindo ao álcool comum, de fórmula CH3 – CH2OH, conhecido como álcool etílico e de nome oficial etanol. Além de estar presente nas bebidas “alcoólicas”, o etanol tem largo emprego industrial – como solvente, na produção de loções e perfumes e, ainda, como combustível para automóveis. A família dos alcoóis, no entanto, é muito mais numerosa e diversificada. Por exemplo, são alcoóis (ou têm o grupo funcional dos alcoóis) substâncias como: a glicerina, usada em sabões, em cosméticos, nas tintas de impressão gráfica, como aditivo em alimentos etc.; os açúcares, como a glicose, a sacarose etc.; o amido, existente na batata, na mandioca, no trigo etc.; a celulose, presente no papel que usamos diariamente; etc
Nomenclatura (IUPAC)
A denominação é realizada trocando-se o final o do nome do hidrocarboneto correspondente pelo sufixo ol. A posição do grupo hidroxila (-OH) deve ser indicada pelo menor número possível.
- A numeração da cadeia principal começa da ponta mais próxima à hidroxila. Se a hidroxila estiver exatamente no meio da cadeia, a numeração deverá ser feita de acordo com a insaturação, e por último, pela ramificação.
Exemplos:

met + an + ol = metanol (um carbono, ligação simples (na verdade, não há ligação entre carbonos pois só existe um carbono no composto), OL pois é um álcool)

et + an + ol = etanol (dois carbonos, ligação simples, e OL porque é um álcool)

prop + an + ol = propanol-1 (três carbonos, ligação simples, e OL porque é um álcool, o 1 indica a posição da hidroxila)

prop + an + ol = propanol-2 (três carbonos, ligação simples, e OL porque é um álcool, o 2 indica a posição da hidroxila)

2,4-dimetil-3-pentanol
2,4 = posições dos radicais metil
3 = posição da hidroxila
pent + an + ol = quantidade de carbonos da cadeia principal + tipo das ligações + OL
Nomenclatura usual
A nomenclatura usual é bastante limitada, somente usada nos compostos que são comumente usados em laboratórios:
Álcool radical+ico
Exemplos:
- Álcool metílico (metanol)
- Álcool etílico (etanol)
- Álcool isopropílico (propanol-2)
*Outra nomenclatura, mais antiga, é a nomenclatura de Kolbe. Esse cientista chamava o metanos de carbinol e considerava os demais alcoóis como seus derivados.
CH3OH carbinol
- Propriedades físicas
Os álcoois geralmente são líquidos (no máximo 10 carbonos no composto) ou sólidos (mais de 10 carbonos).
- Solubilidade em água
A única parte polar dos álcoois é o grupo OH (hidroxila), por isso, quanto mais carbonos o álcool tiver, menor será a solubilidade, pois “semelhante dissolve semelhante” (a água é polar).
- Pontos de fusão e ebulição
Quanto maior for a cadeia do composto, maior será seu ponto de fusão e de ebulição.
Classificação dos alcoóis
Os alcoóis podem ser classificados segundo vários critérios. Os mais comuns são:
· De acordo com a cadeia carbônica
CH3 – CH2 – CH2OH CH2 = CH – CH – CH3
|
propan-1-ol OH
(álcool saturado) 1-buten-3-ol
(álcool insaturado)
· De acordo com o número de oxidrilas
São os compostos que apresentam apenas uma hidroxila. Exemplo:
CH3-CH2-OH (etanol)
CH3-CH2-CH2-OH (propanol-1)
A hidroxila em monoálcoois pode estar ligada à carbono primário, secundário ou terciário, formando assim, álcool primário, secundário e terciário, respectivamente.
- diálcoois ou dióis
Possuem duas hidroxilas. Exemplo:
HO-CH2-CH2-OH
Obs: não existem álcoois com duas hidroxilas no mesmo carbono. Quando isso acontece, o composto fica instável, e transforma-se em aldeídos.
- triálcoois ou trióis
Possuem três hidroxilas. Exemplo:

e assim por diante: tetróis, pentóis, polióis etc.
· De acordo com a posição da oxidrila
-Álcoois primários – apresentam sua hidroxila ligada a carbono na extremidade da cadeia. Possuindo um grupo característico – CH2OH. -Álcoois secundários – apresentam sua hidroxila unida a carbono secundário da cadeia. Possuindo o grupo característico – CHOH.
- Álcoois terciários – apresentam sua hidroxila ligada a carbono terciário. Possuindo o grupo – COH.
A presença dos alcoóis em nossa vida
Metanol
O metanol, ou ainda o álcool da madeira, pode ser preparado pela destilação seca de madeiras, seu processo mais antigo de obtenção, e de onde, durante muito tempo, foi obtido exclusivamente.
Atualmente é obtido pela reação do gás de síntese (produzido a partir de origens fósseis, como o gás natural), uma mistura de H2 com CO passando sobre um catalisador metálico a altas temperaturas e pressões.
Esta reação é uma redução catalítica do monóxido de carbono, e processa-se a temperatura de cerca de 300°C e pressões de 200 a 300 atm. É utilizado como catalisador uma mistura de óxidos metálicos como óxido de cromo (III) (Cr2O3) e óxido de zinco (ZnO).
A equação da reação é:
CO + 2 H2 → H3C-OH
Usos
O metanol é principalmente um solvente industrial, pois ele dissolve alguns sais melhor do que o etanol; é utilizado na indústria de plásticos, na extração de produtos animais e vegetais, e como solvente em reações de importância farmacológica, como no preparo de colesterol, vitaminas e hormônios. É matéria prima na produção de formaldeído.
É usado como combustível em algumas categorias de monopostos dos EUA (ex: Champ Car, IRL, Dragster). As equipes e o piloto são instruidos de como agir diante de um incêndio provocado por um acidente. Como o fogo não é visível é preciso jogar água em todos os cantos onde supostamente está ocorrendo e no próprio piloto e membros da equipe se for o necessário.
Etanol
O etanol (álcool etílico) é um álcool derivado de cereais e vegetais. No Brasil, utiliza-se a cana-de-açúcar para a produção do etanol, enquanto nos Estados Unidos e México é utilizado o milho.
É utilizado na fabricação de bebidas alcoólicas fermentadas (cerveja, aguardente, vinho), produtos de limpeza doméstica e também de combustíveis para automóveis.
Tipos e usos
- Anidro - o álcool anidro é bastante caracterizado pelo teor alcólico mínimo de 99,3° (INPM), sendo composto apenas de etanol ou álcool etílico. É utilizado como combustível para veículos (Gasolina C) e matéria prima na indústria de tintas, solventes e vernizes.
- Hidratado - é uma mistura hidroalcólica com teor alcoólico mínimo de 92,6° (INPM), composto por álcool etílico ou etanol. O emprego de álcool hidratado é na indústria farmacêutica, alcoolquímica e de bebidas, combustível para veículos e produtos para limpeza. O etanol é também usado como matéria prima para a produção de vinagre e ácido acético, a síntese de cloral e iodofórmio.
Bebidas alcoólicas
O sistema nervoso central é o órgão onde o etanol tem ação mais rápida, causando sedação, redução de ansiedade, fala arrastada, ataxia, desinibição e redução da capacidade de julgamento. Apesar de muitas pessoas pensarem que o álcool é estimulante, na verdade trata-se de um depressor do SNC. A estimulação que ocorrem em pequenas doses é decorrente da depressão no cérebro dos mecanismos de inibição.
Os fatores para alteração no comportamento do indivíduo, cognição e descoordenação motora depende do sexo, da dose, da velocidade de absorção e a tolerância desenvolvida.
Algumas pessoas após ingerirem quantidade considerável de bebida, tornam-se falantes enquanto outras retraem-se, tem mau-humor, irritação ou introspecção. Também pode ocorrer perda de controle e agressividade.
Na prática clínica, a detecção de casos de alcoolismo geralmente é caracterizada pelo rubor facial, fala pastosa, ataxia, nistagmo irritabilidade e dificuldade de concentração, e é classificada pela CID-10 (intoxicação aguda). Se a pessoa atingir sinais de intoxicação com quantidade de álcool menor o diagnóstico é dado como intoxicação patológico.
Dependendo da dose ingerida a pessoa pode ter amnésia.
Fora isto muitos consomem o etanol com energéticos, como os da marca Red Bull que é um estimulante correndo o risco de existir uma reação antagonista ou apenas mascarante de embriaguez.Todos energéticos possuem na embalagem orientação para evitar o consumo deles com qualquer tipo de bebida alcoólica. O alcoolismo é uma doença crônica, caracterizada pela dependência de etanol. Na prática clínica, constata-se que o alcoólatra cada vez mais depende da substância para viver, desenvolvendo grave dependência física quando este é retirado.
Bafômetro
Lei seca sendo aplicada
O motorista deve assoprar o bafômetro com força no canudinho, que conduzirá o ar de seus pulmões para um analisador contendo uma solução ácida de dicromato de potássio.
O princípio de detecção do grau alcóolico no corpo humano está fundamentado na avaliação das mudanças das características elétricas de um sensor sob os efeitos provocados pelos resíduos do álcool etílico no hálito do indivíduo.
O sensor é um elemento formado por um material cuja condutividade elétrica é influenciada pelas substâncias químicas do ambiente que se aderem à sua superfície. Sua condutividade elétrica diminui quando a substância é o oxigênio e aumenta quando se trata de álcool. Entre as composições preferidas para formar o sensor destacam-se aquelas que utilizam polímeros condutores ou filmes de óxidos cerâmicos, como óxido de estanho (SnO2), depositados sobre um substrato isolante.
A correspondência entre a concentração de álcool no ambiente, medida em partes por milhão (ppm), e uma determinada condutividade elétrica é obtida mediante uma calibração prévia onde outros fatores, como o efeito da temperatura ambiente, o efeito da umidade relativa, regime de escoamento de ar etc., são rigorosamente avaliados. A concentração de álcool no hálito das pessoas está relacionada com a quantidade de álcool presente no seu sangue dado o processo de troca que ocorre nos pulmões.
O álcool presente no "bafo", é convertido em ácido acético conforme mostra a reação abaixo:
3CH3CH2OH + 2K2Cr2O7 + 8H2SO4 - > 3CH3COOH + 2Cr2(SO4)3 + 2K2SO4 +11H2O
Nesta reação o etanol é convertido a ácido acético e o cromo, na forma de íon cromato (amarelo alaranjado) é transformado em Cr + 3 (coloração verde).Quanto maior a concentração de álcool mais intensa é a coloração esverdeada obtida.
Alunas: Renara Resende (34) / Rafaela Teixeira (32)
Escola Estadual Sérgio de Freitas Pacheco 3º “A"
Professora: Miramar
Tema: Álcoois





Nenhum comentário:
Postar um comentário